Научная группа профессора И.А. Баловой
Научная группа кафедры органической химии
Лаборатории: 4072, 4073, 4076, 4083
Химия ацетиленовых соединений
Состав группы
Руководитель
 |
Ирина Анатольевна Баловад.х.н, директор Института химии |
Сотрудники
 |
Говди Анастасия Иосифовнак.х.н., доцент |
 |
Данилкина Наталья Александровнак.х.н., доцент |
 |
Ефремова Мария Михайловнак.х.н., доцент кабинеты: 4128, 4124 |
 |
Сорокоумов Виктор Николаевичк.х.н., доцент председатель Учебно-Методической комиссии Института химии |
 |
Каминский Никита Андреевичмагистр химии, инженер-исследователь |
Студенты и аспиранты (кафедра органической химии)
 |
Видякина Александра Александровна2 курс аспирантуры |
 |
Хмелевская Екатерина Алексеевна2 курс аспирантуры |
 |
Диденко Егор Александрович2 курс магистратуры |
 |
Ким Миа Деновна1 курс магистратуры |
 |
Огурцова Анна Дмитриевна1 курс магистратуры |
 |
Королёв-Зелёный Кирилл Владиславович4 курс бакалавриата |
 |
Кутузов Ярослав Александрович4 курс бакалавриата |
 |
Галкин Егор Сергеевич3 курс бакалавриата |
 |
Евсюков Илья Валерьевич2 курс бакалавриата |
 |
Менчиков Василий Владиславович2 курс бакалавриата |
 |
Хашимова Диана Давлатовна2 курс бакалавриата |
 |
Мельников Владимир Евгеньевич1 курс бакалавриата |
Тематика группы
- Разработка подходов к синтезу фунцкционализированных моно- и диацетиленовых соединений.
- Применение ацетиленовых соединений в синтезе гетероциклов.
- Разработка методов получения аналогов ендииновых антибиотиков и изучение их химических и биологических свойств.
- Разработка подходов к синтезу напряженных циклоалкинов как реагентов для click-реакций и биоортогональной химии.
- Получение и изучение свойств новых каталитических систем на основе диаминокарбеновых комплексов палладия в реакциях Соногаширы-Хагихары, Сузуки-Мияуры, Бухвальда-Хартвига.
- Синтез новых флуоресцирующих полиариленэтиниленовых полимеров, изучение их свойств и области применения.
Основные научные направления
Направление 1 — Ацетиленовые соединения в органическом синтезе и создании на их основе веществ с полезными свойствами
(A) Разработка подходов к синтезу фунцкционализированных диацетиленовых соединений
Среди методов получения терминальных диинов особое место занимает реакция «диацетиленовой молнии» [A] — открытый в нашей научной группе уникальный процесс одновременного перемещения двух сопряженных тройных связей из интернального положения в терминальное под действие 2-аминоэтанамида лития. Данная реакция может быть использована как для нефункционализированных алкадиинов, так и в ряду диацетиленовых спиртов. [B] [1]
«Диацетиленовая молния» с последующей функционализацией была успешно применена в синтезе кетонов, [2] диацетиленовых спиртов, [C] [D] карбоновых кислот [D], тетраинов [E] и других производных.
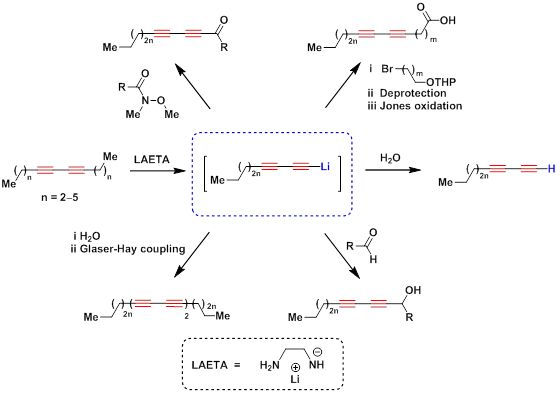
В тандеме с реакцией Соногаширы, [3][4][5][6][1][7][8] диацетиленовая молния является уникальным синтетическим методом для получения арил- и гетероарилдиацетиленов.
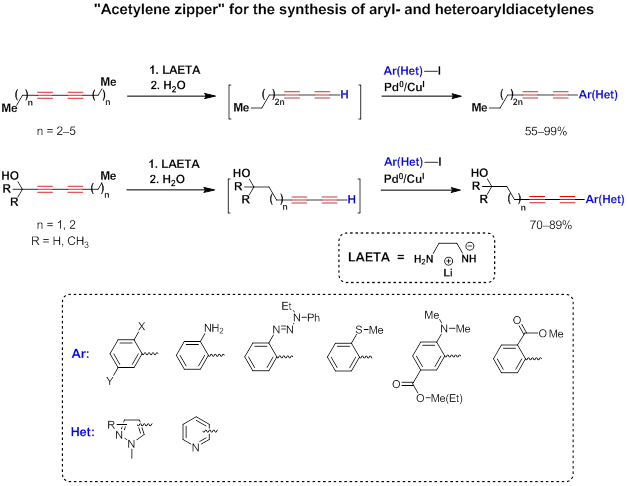
Вторым методом получения терминальной диацетиленовой функции является удаление защитных групп. Наиболее мягкие условия используются для удаления триметилсилильной (ТМС) защитной группы. Десилилирование ТМС-диацетиленов под действием KF и реакция Соногаширы в условиях one-pot оказались удобным методом получения функционализированных аренов, содержащих диацетиленовый фрагмент.[9]
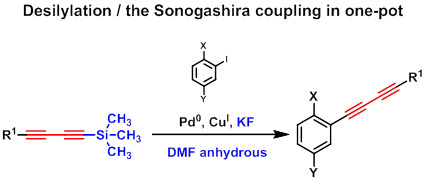
(B) Диацетиленовые соединения в синтезе гетероциклов
Две сопряженные тройные связи наделены поистине безграничным синтетическим потенциалом. Исследования, проводимые в нашей группе, показали, что арилдиацетилены, содержащие в орто-положении к тройным связям гетероатомную функциональную группу, способны претерпевать гетероциклизации с участием лишь одной тройной связи (электрофил промотируемую циклизацию,[10][11][12] циклизацию Рихтера [13][14][5]), давая гетероциклы, содержащие и тройную связь, и атом галогена при соседних атомах углерода. Данный способ был впервые использован в нашей группе для получения синтетически важных иодэтинилбензотиофенов, -бензофуранов, -индолов, -изокумаринов и бромэтинилциннолинов. Кроме этого, недавно нами было установлено, что медь-катализируемое азид-алкиновое циклоприсоединение (CuAAC) 1-иодбута-1,3-диинов к органическим азидами является эффективным методом получения 5-иод-4-этинил[1,2,3]триазолов. [15]
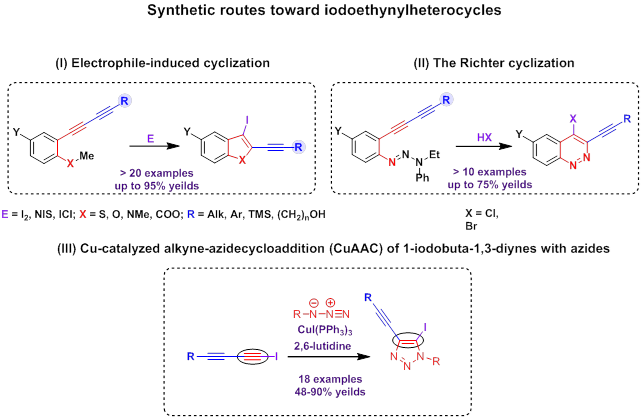
Обе функциональные группы (тройная связь и атом галогена) чрезвычайно важны для дальнейшей функционализации гетероциклических молекул. Все три метода синтеза иодэтинилгетероциклов легли в основу предложенной в нашей группе стратегии синтеза гетероциклических аналогов природных ендииновых антибиотиков.
(С) Синтез и свойства аналогов ендииновых антибиотиков
Ендииновые антибиотики — соединения, обладающие высокой противоопухолевой и антибактериальной активности благодаря способности (Z)-3-ен-1,5-дииновой системы, включенной в 9- или 10-членный цикл, претерпевать циклоароматизацию Бергмана с образованием 1,4-фенилендирадикалов, разрушающих молекулы ДНК.
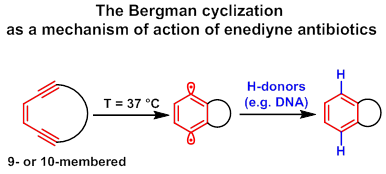
В нашей группе ведется поиск простейших аналогов природных ендииновых антибиотиков, аннелированных с гетероциклами. Разработанный нами способ синтеза иодоэтинилгетероциклов при комбинации с реакцией Соногаширы позволяет вводить в соседние положения гетероцикла ацетиленовые фрагменты с четко заданными функциональными группами. В свою очередь, это открывает возможность синтеза нужных исходных соединений для макроциклических ендииновых систем, в зависимости от того, какой метод макроциклизации будет выбран. Для синтеза ендиинов нами изучены границы применения макроциклизации при помощи макроциклизации по Нозаки,[16][17] метатезиса алкенов,[11] [18] и реакции Николаса.[19][20][21]
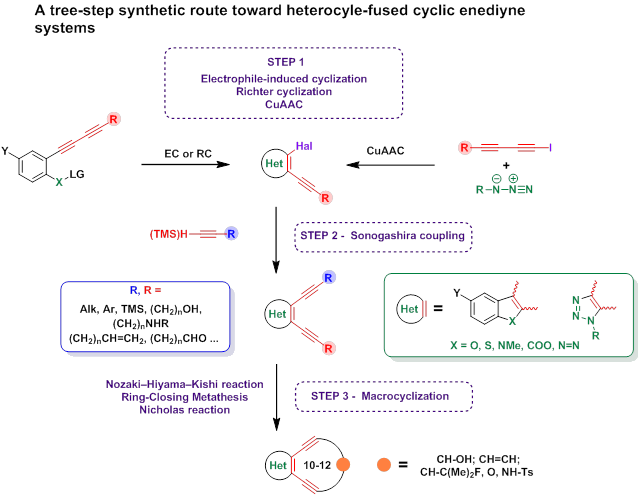
На сегодняшний день реакция Николаса оказалась наиболее универсальной для этих целей и позволила верифицировать шкалу относительной реакционной способности ендиинов, конденсированных с бензотиофеном.[20]
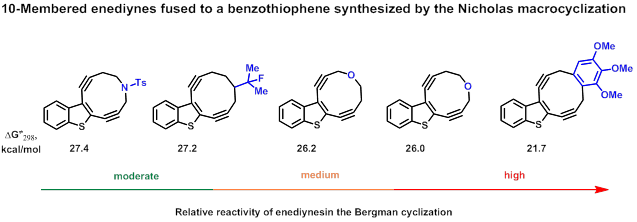
При сотрудничестве с кафедрой генетики и биотехнологии биологического факультета СПбГУ нами было установлено, что 10-членные ендиины способны генерировать 1- и 2-цепочечные разрывы ДНК, что крайне важно для поиска в этом ряду новых противоопухолевых соединений.
В настоящее время в группе проводятся работы по синтезу небольшой базы 10-членных ендиинов, конденсированных с различным гетероциклами.
Синтез новых флуоресцирующих полиариленэтиниленовых полимеров
Сегодня полиариленэтинилены являются перспективной группой для создания полимеров с четко заданными свойствами. Так, для полиариленэтиниленов, в структуре которых имеются группы, способные избирательно связываться с аналитами, после связывания с аналитом наблюдается эффект гашения флуоресценции. Такие полимеры интересны для создания детекторных систем. В нашей группе были получены полиариленэтинилены, содержащие циннолиновые фрагменты, способные проявлять эффект гашения флуоресценции в присутствии ионов PdII.[22] Планируется создание полиариленэтиниленов, содержащих бензотиофеновые и триазольные фрагменты.
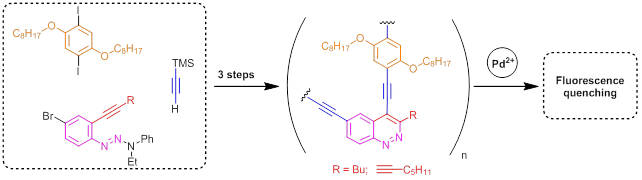
Направление 2 — Новые катализаторы и их использование в синтезе ацетиленовых соединений
Для эффективного осуществления «атом-экономичных» превращений при создании новых углерод-углеродных и углерод-гетероатомных связей в ряду производных ацетилена и органических соединений других классов в нашей группе ведутся исследования по разработке эффективных гомогенных и гетерогенных каталитических систем.
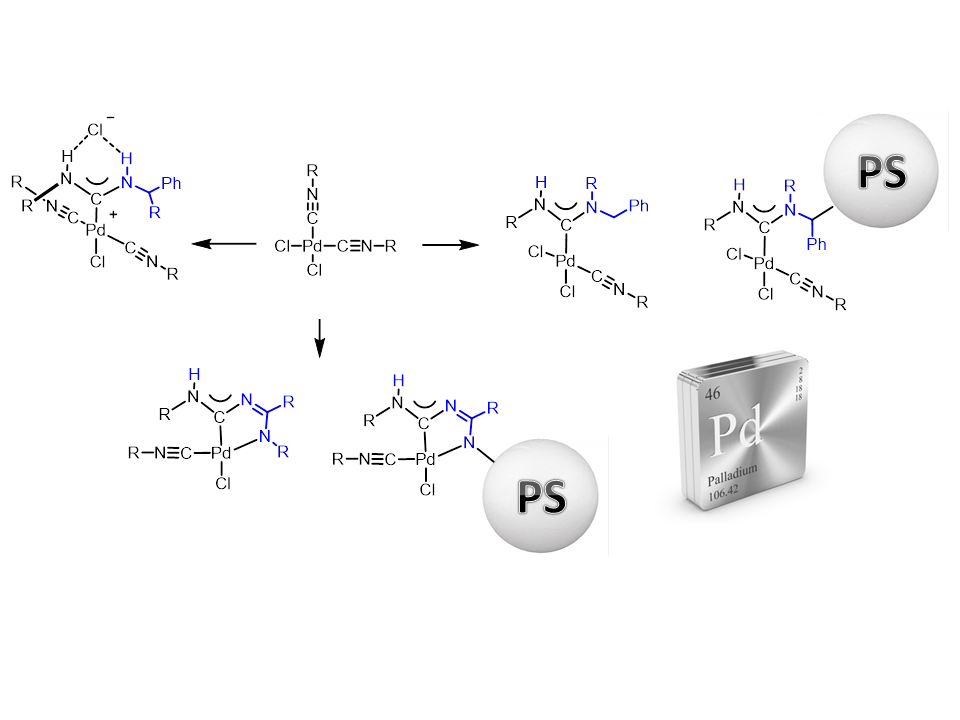
В работе можно выделить два взаимозависимых направления:
- исследование высокоактивных гомогенных катализаторов на основе диаминокарбеновых комплексов палладия, способных эффективно работать в условиях низких каталитических концентраций;
- развитие регенерируемых катализаторов путем иммобилизации высокоактивных гомогенных комплексов палладия на подходящем носителе,[23] который инертен в используемых условиях реакции.
В настоящее время с помощью металл-промотируемой реакции нуклеофильного присоединения амино- и амидиновых групп к изоцианидам в составе комплексов палладия (II) разработан метод получения эффективных гетерогенных каталитических систем на основе ациклических диаминокарбеновых комплексов палладия,[24] проявляющих высокую активность в условиях реакций Соногаширы и Сузуки на широком наборе субстратов, с возможностью многократного использования каталитических систем без существенной потери каталитической активности.
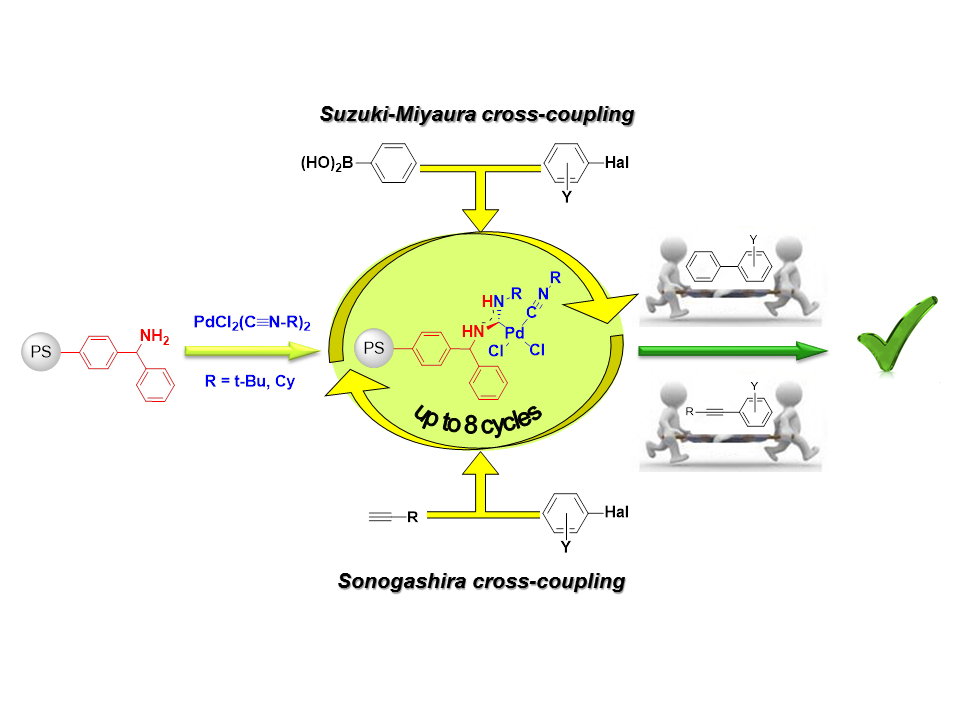
В рамках проводимого нами исследования было показано,[25] что основной вклад в каталитическую активность гетерогенных прекатализаторов на основе ациклических диаминокарбеновых комплексов палладия вносит палладий, обратимо вымываемый в раствор с носителя в процессе реакции за счет нового пути активации PdII – Pd0 через образование карбодиимида.
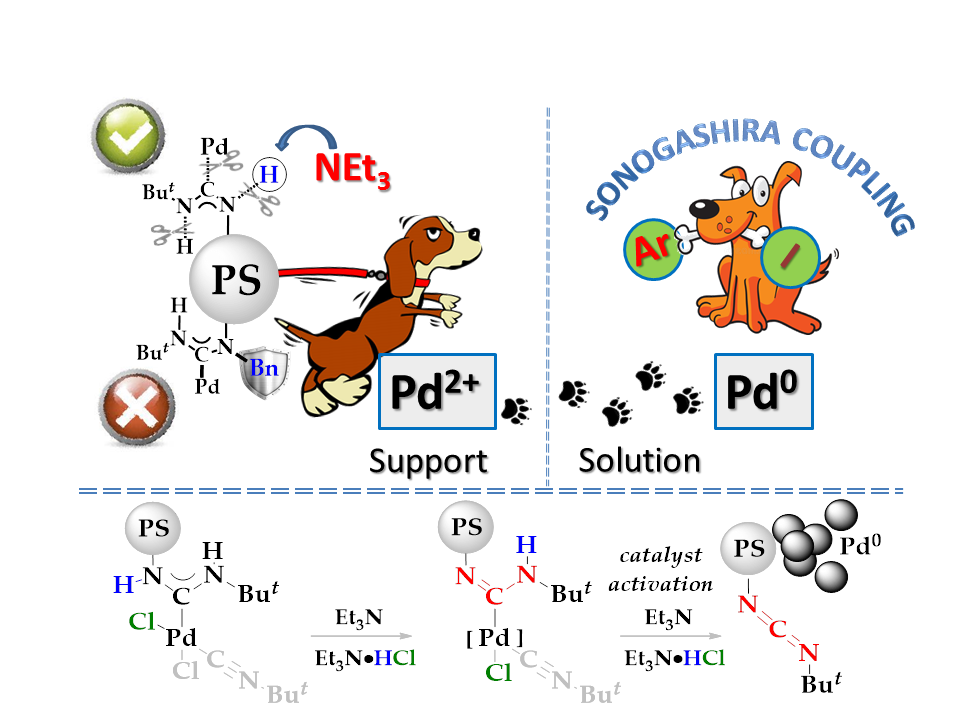
Наши результаты показывают принципиально новый путь генерации и стабилизации Pd0-видов и проливают свет на характер катализа для комплексов палладия с различными диаминокарбеновыми лигандами. Легкость удаления карбодиимида и HCl с образованием каталитически активного Pd0 из разработанных прекатализаторов может стать хорошей альтернативой активации коммерчески доступных прекатализаторов Бухвальда.
В научной группе также ведутся разработки перспективных каталитических систем, способных катализировать реакции с участием малореакционоспособных коммерчески важных арилхлоридов в мягких условиях (при комнатной температуре без использования сильных оснований).
Направление 3 — Разработка новых ингибиторов протеинфосфотирозинфосфатазы 1В на основе производных 4-оксо-1,4-дигидроциннолина
Фермент протеинфосфотирозинфосфатаза 1В (ПФТФ1В) является важнейшим негативным регулятором инсулиновой и лептиновой систем, которые активируются через тирозинкиназные механизмы. Повышение активности ПФТФ1В ведет к инсулиновой (ИР) и лептиновой резистентности (ЛР) и является причиной ожирения, сахарного диабета и других метаболических расстройств. В связи с этим актуальной задачей эндокринологии является расшифровка механизмов действия ПФТФ1В с помощью функциональных зондов и разработка ее селективных ингибиторов, применение которых является многообещающим подходом для лечения метаболических расстройств, связанных с ИР и ЛР. Наиболее перспективным направлением в разработке ингибиторов ПФТФ1В является создание «бинарных» ингибиторов, которые взаимодействуют с каталитическим (низкоспецифичным) и аллостерическим (высокоспецифичным) сайтами ПФТФ1В, что обеспечивает высокую эффективность и селективность их действия.
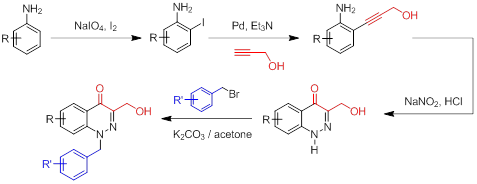
Нами было предложено использовать производные 4-оксо-1,4-дигидроциннолина как специфичные ингибиторы ПФТФ1В. Разработанный подход к синтезу с использованием реакции Соногаширы для получения орто-этинилзамещенных анилинов и реакция Рихтера для формирования циннолинового ядра, позволяет получать подобные производные с хорошими выходами за малое число стадий. Кроме того, были получены предварительные результаты [26] об эффективности впервые синтезированного производного 4-оксо-1,4-дигидроциннолина – этилового эфира 3-(гидроксиметил)-4-оксо-1,4-дигидроциннолин-6-карбоновой кислоты как специфичного ингибитора ПФТФ1В в условиях in vitro и in vivo. Было показано, что при обработке первичной культуры гипоталамических нейронов крысы с помощью этилового эфира 3-(гидроксиметил)-4-оксо-1,4-дигидроциннолин-6-карбоновой кислоты происходит усиление стимулирующего эффекта лептина на фосфорилирование Akt-киназы и STAT3-белка, что свидетельствует о подавлении активности ПФТФ1В, которая негативно регулирует эффекты лептина. Наряду с этим, это производное 4-оксо-1,4-дигидроциннолина при курсовом введении крысам вызывало снижение аппетита, массы тела, жировой ткани, улучшало метаболические показатели и повышало чувствительность к инсулину у крыс с экспериментальной моделью ожирения.
Литература
- Балова И. А., Ремизова Л.А., Фаворская И.А. Прототропная изомеризация диацетиленовых соединений. ЖОрХ, 1986, 22 (11) 2459−2460.
- И.А.Балова, И.В.Захарова, Л. А. Ремизова. Прототропная изомеризация диацетиленовых спиртов. ЖОрХ, 1993, 29(9), 1732-1738.
- Балова И. А., Морозкина С. Н., Воскресенский С. В., Ремизова Л. А. Последовательные реакции диацетиленов: «ацетиленовая молния» и оксиалкилирование 1-литио-1,3-диинов как путь синтеза α- и β- диацетиленовых спиртов. ЖОрХ , 2000, 36 (10), 1466.
- И.А. Балова, Л.А. Ремизова, В.Ф. Макарычева, Е.Г. Румянцева, И.А. Фаворская. Синтез длинноцепных диацетиленовых спиртов. ЖОрХ, 1991, 27 (1), 64-66.
- И.А.Балова, Л. А. Ремизова. Реакция ацетиленовой молнии диацетиленовых соединений в синтезе тетраинов. ЖОрХ, 1994, 30 (2), 207-9.
- Kulyashova, A.E.; Sorokoumov, V.N.; Popik, V. V; Balova, I.A. An acetylene zipper—Sonogashira reaction sequence for the efficient synthesis of conjugated arylalkadiynols. Tetrahedron Lett. 2013, 54, 2235–2238, https://linkinghub.elsevier.com/retrieve/pii/S004040391300316X
- Novikov, R. V; Vasil’ev, A.A.; Balova, I.A. Convenient synthesis of dodeca-1,3-diynyl ketones by the “diacetylene zipper” reaction. Russ. Chem. Bull. 2005, 54, 1043–1045, http://link.springer.com/10.1007/s11172-005-0355-8
- Balova, I.A.; Morozkina, S.N.; Knight, D.W.; Vasilevsky, S.F. A one-pot synthesis of 1-arylalka-1,3-diynes by sequential acetylene zipper and Sonogashira reactions. Tetrahedron Lett. 2003, 44, 107–109, http://linkinghub.elsevier.com/retrieve/pii/S0040403902024966
- Balova, I.A.; Sorokoumov, V.N.; Morozkina, S.N.; Vinogradova, O. V; Knight, D.W.; Vasilevsky, S.F. A Convenient Synthesis of Functionalised 1-Aryl-1,3-alkadiynes. Eur. J. Org. Chem. 2005, 2005, 882–888, http://doi.wiley.com/10.1002/ejoc.200400688
- Vinogradova, O. V.; Sorokoumov, V.N.; Balova, I.A. A short route to 3-alkynyl-4-bromo(chloro)cinnolines by Richter-type cyclization of ortho-(dodeca-1,3-diynyl)aryltriaz-1-enes. Tetrahedron Lett. 2009, 50, 6358–6360, http://dx.doi.org/10.1016/j.tetlet.2009.08.103
- Sorokoumov, V.N.; Popik, V. V.; Balova, I.A. Access to 2,3-bis(buta-1,3-diynyl)pyridines. Mendeleev Commun. 2011, 21, 19–20, https://linkinghub.elsevier.com/retrieve/pii/S0959943611000095
- Govdi, A.I.; Kulyashova, A.E.; Vasilevsky, S.F.; Balova, I.A. Functionalized buta-1,3-diynyl- N -methylpyrazoles by sequential “diacetylene zipper” and Sonogashira coupling reactions. Tetrahedron Lett. 2017, 58, 762–765, http://dx.doi.org/10.1016/j.tetlet.2017.01.032
- Kulyashova, A.E.; Mikheeva, E. V.; Danilkina, N.A.; Balova, I.A. Synthesis of 2-(buta-1,3-diynyl)-N,N-dimethylanilines Using Reductive Methylation Step. Mendeleev Commun. 2014, 24, 102–104, http://dx.doi.org/10.1016/j.mencom.2014.03.013
- Lyapunova, A.G.; D’yachenko, A.S.; Danilkina, N.A. Potassium fluoride for one-pot desilylation and the Sonogashira coupling of ethynylsilanes and buta-1,3-diynylsilanes. Russ. J. Org. Chem. 2017, 53, 800–804, http://link.springer.com/10.1134/S1070428017050268
- Danilkina, N.; Bräse, S.; Balova, I. Electrophilic Cyclization of Buta-1,3-diynylarenes: Synthesis of Precursors of (Z)-3-Ene-1,5-diyne Systems Fused to Heterocycles. Synlett 2011, 2011, 517–520, http://www.thieme-connect.de/DOI/DOI?10.1055/s-0030-1259547
- Danilkina, N.A.; Kulyashova, A.E.; Khlebnikov, A.F.; Bräse, S.; Balova, I.A. Electrophilic Cyclization of Aryldiacetylenes in the Synthesis of Functionalized Enediynes Fused to a Heterocyclic Core. J. Org. Chem. 2014, 79, 9018–9045, http://pubs.acs.org/doi/10.1021/jo501396s
- Danilkina, N.A.; Gurskaya, L.Y.; Vasilyev, A. V.; Balova, I.A. Towards Isocoumarin-Fused Enediyne Systems through the Electrophilic Cyclization of Methyl o -(Buta-1,3-diynyl)benzoates. Eur. J. Org. Chem. 2016, 2016, 739–747, http://doi.wiley.com/10.1002/ejoc.201501262
- Vinogradova, O. V.; Sorokoumov, V.N.; Vasilevsky, S.F.; Balova, I.A. The Richter reaction of ortho-(alka-1,3-diynyl)aryldiazonium salts. Tetrahedron Lett. 2007, 48, 4907–4909, https://linkinghub.elsevier.com/retrieve/pii/S0040403907009203
- Vinogradova, O. V.; Sorokoumov, V.N.; Vasilevskii, S.F.; Balova, I.A. Studies on cyclization of o-(alka-1,3-diynyl)arenediazonium salts. Russ. Chem. Bull. 2008, 57, 1725–1733, http://link.springer.com/article/10.1007/s11172-008-0228-z
- Govdi, A.I.; Danilkina, N.A.; Ponomarev, A. V.; Balova, I.A. 1-Iodobuta-1,3-diynes in Copper-Catalyzed Azide–Alkyne Cycloaddition: A One-Step Route to 4-Ethynyl-5-iodo-1,2,3-triazoles. J. Org. Chem. 2019, 84, 1925–1940, http://pubs.acs.org/doi/10.1021/acs.joc.8b02916
- Kulyashova, A.E.; Ponomarev, A.V.; Selivanov, S.I.; Khlebnikov, A.F.; Popik, V.V.; Balova, I.A. Cr(II)-promoted internal cyclization of acyclic enediynes fused to benzo[ b ]thiophene core: Macrocycles versus 2-methylenecycloalkan-1-ols formation. Arab. J. Chem. 2018, https://doi.org/10.1016/j.arabjc.2018.05.005
- Vinogradova, O. V.; Balova, I.A.; Popik, V. V. Synthesis and Reactivity of Cinnoline-Fused Cyclic Enediyne. J. Org. Chem. 2011, 76, 6937–6941, http://pubs.acs.org/doi/abs/10.1021/jo201148h
- Danilkina, N.; Nieger, M.; Selivanov, S.; Bräse, S.; Balova, I. Electrophilic Cyclization and Ring-Closing Metathesis as Key Steps in the Synthesis of a 12-Membered Cyclic Enediyne. Eur. J. Org. Chem. 2012, 2012, 5660–5664, http://doi.wiley.com/10.1002/ejoc.201200881
- Lyapunova, A.G.; Danilkina, N.A.; Khlebnikov, A.F.; Köberle, B.; Bräse, S.; Balova, I.A. Oxaenediynes through the Nicholas-Type Macrocyclization Approach. Eur. J. Org. Chem. 2016, 2016, 4842–4851, http://doi.wiley.com/10.1002/ejoc.201600767
- Lyapunova, A.G.; Danilkina, N.A.; Rumyantsev, A.M.; Khlebnikov, A.F.; Chislov, M. V.; Starova, G.L.; Sambuk, E. V.; Govdi, A.I.; Bräse, S.; Balova, I.A. Relative Reactivity of Benzothiophene-Fused Enediynes in the Bergman Cyclization. J. Org. Chem. 2018, 83, 2788–2801, http://pubs.acs.org/doi/10.1021/acs.joc.7b03258
- Danilkina, N.; Rumyantsev, A.; Lyapunova, A.; D’yachenko, A.; Khlebnikov, A.; Balova, I. 10-Membered Azaenediyne Fused to a Benzothiophene through the Nicholas Macrocyclization: Synthesis and DNA Cleavage Ability. Synlett 2019, 30, 161–166, http://www.thieme-connect.de/DOI/DOI?10.1055/s-0037-1610352
- Danilkina, N.A.; Vlasov, P.S.; Vodianik, S.M.; Kruchinin, A.A.; Vlasov, Y.G.; Balova, I.A. Synthesis and chemosensing properties of cinnoline-containing poly(arylene ethynylene)s. Beilstein J. Org. Chem. 2015, 11, 373–384, http://www.beilstein-journals.org/bjoc/content/11/1/43
- Mikhaylov, V.N.; Sorokoumov, V.N.; Balova, I.A. Polystyrene-supported diaminocarbene complexes of palladium(II): synthesis, characterization and application as a precatalyst in Sonogashira–Hagihara and Suzuki–Miyaura cross coupling. Russ. Chem. Rev. 2017, 86, 459–473, http://stacks.iop.org/0036-021X/86/i=6/a=459?key=crossref.3ea2445ecd754502db2a71e84887b220
- Mikhaylov, V.N.; Sorokoumov, V.N.; Korvinson, K.A.; Novikov, A.S.; Balova, I.A. Synthesis and Simple Immobilization of Palladium(II) Acyclic Diaminocarbene Complexes on Polystyrene Support as Efficient Catalysts for Sonogashira and Suzuki–Miyaura Cross-Coupling. Organometallics 2016, 35, 1684–1697, https://pubs.acs.org/doi/10.1021/acs.organomet.6b00144
- Mikhaylov, V.; Sorokoumov, V.; Liakhov, D.; Tskhovrebov, A.; Balova, I. Polystyrene-Supported Acyclic Diaminocarbene Palladium Complexes in Sonogashira Cross-Coupling: Stability vs. Catalytic Activity. Catalysts 2018, 8, 141, http://www.mdpi.com/2073-4344/8/4/141
- Zakharova, I.O.; Sorokoumov, V.N.; Bayunova, L. V; Derkach, K. V; Shpakov, A.O. 4-oxo-1,4-dihydrocinnoline Derivative with Phosphatase 1B Inhibitor Activity Enhances Leptin Signal Transduction in Hypothalamic Neurons. J. Evol. Biochem. Physiol. 2018, 54, 273–280, http://link.springer.com/10.1134/S0022093018040038
Публикации
2023
- A.A. Vidyakina, A. A. Shtyrov, M.N. Ryazantsev, A. F. Khlebnikov, I. E. Kolesnikov, V. V. Sharoyko. D. V. Spiridonova, I. A. Balova, S. Bräse, N. A. Danilkina. Development of Fluorescent Isocoumarin-Fused Oxacyclononyne – 1,2,3-Triazole Pairs. Chemistry — A European Journal, 2023, e202300540. Статья находится в открытом доступе и попала в Hot Topic: Click Chemistry издательства Wiley: 10.1002/(ISSN)1521-3773.hottopic-clickchemistry.
- A. A. Babushkina, V. N. Mikhailov. A. D. Ogurtsova, A. S. Bunev, V.N. Sorokoumov, I. A. Balova. The Richter reaction in the synthesis of combretastatin analogs. Russian Chemical Bulletin. 2023, 72(4), 1012-1022. DOI: 10.1007/s11172-023-3866-3.
- A. I. Govdi, S. O. Anisimov, N. A. Danilkina, A. S. Bunev. I. A. Balova. Acyclic enediynes fused to triazoleand benzothiophene containing propargylamine moieties. Mendeleev Commun., 2023, 33, 328–330. DOI: 10.1016/j.mencom.2023.04.010.
- K. V. Derkach, M. A. Gureev, A. A. Babushkina, V. N. Mikhaylov , I. O. Zakharova, A. A. Bakhtyukov, V. N. Sorokoumov, A. S. Novikov, M. Krasavin, A. O. Shpakov, I. A. Balova. Dual PTP1B/TC-PTP Inhibitors: Biological Evaluation of 3-(Hydroxymethyl)cinnoline-4(1H)-Ones, Int. J. Mol. Sci. 2023, 24(5), 4498; DOI: 10.3390/ijms24054498.
- Bakhtyukov A.A., Derkach K.V., Fokina E.A. , Lebedev I.A., Sorokoumov V.N., Bayunova, L.V., Shpakov A.O., / Effect of Different Luteinizing Hormone Receptor Agonists on Ovarian Steroidogenesis in Mature Female Rats. / J Evol Biochem Phys 59, 57–68 (2023). DOI: 10.1134/S0022093023010052.
- Fokina E.A., Derkach K.V., Bakhtuykov A.A., Sorokoumov V.N., Lebedev I.A., Morina I.Y., Shpakov A.O. / Stimulation Of Ovulation In Immature Female Rats Using Orthosteric And Allosteric Luteinizing Hormone Receptor Agonists / Doklady Rossijskoj akademii nauk. Nauki o žizni. – (2023). - Vol. 508. - N. 1. - P. 30-34. doi: 10.31857/S2686738922700032.
- Efremova M.М., Rumyantsev A.M., Babitova E.S., Ianshina T. M., Govd A.I. Synthesis of 5-ethynylisoxazoles based on 1,3-dipolar cycloaddition reactions of nitrile oxides with conjugated diynes. Russ. Chem. Bull. 2023, 72, 1717–1721. DOI: 10.1007/s11172-023-3952-5.
- T. Ianshina; A. Sidorin; K. Petrova; M. Shubert, A. Makeeva, E. Sambuk; A. Govdi, A. Rumyantsev, M. Padkina Effect of Methionineon Gene Expression in Komagataella phaffii Cells. Microorganisms. 2023, 11, 877. DOI: 10.3390/microorganisms11040877.
- S.G.Zlotin, K.S.Egorova, V.P.Ananikov, A.A.Akulov, M.V.Varaksin, O.N.Chupakhin, V.N.Charushin...., I.A.Balova, V.N.Sorokoumov et al. Russ. Chem. Rev., 2023, 92 (12) RCR5104.
- Derkach, K.V.; Lebedev, I.A.; Morina, I.Y.; Bakhtyukov, A.A.; Pechalnova, A.S.; Sorokoumov, V.N.; Kuznetsova, V.S.; Romanova, I.V.; Shpakov, A.O., Int. J. Mol. Sci., 24 (2023), 16618.
2022
- Danilkina, N.A.; Khmelevskaya, E.A.; Lyapunova, A.G.; D’yachenko, A.S.; Bunev, A.S.; Gasanov, R.E.; Gureev, M.A.; Balova, I.A. Functionalized 10-Membered Aza- and Oxaenediynes through the Nicholas Reaction. Molecules 2022, 27, 6071, doi: 10.3390/molecules27186071. Impact Factor: 4.927.
- Babushkina, A.A.; Mikhaylov, V.N.; Novikov, A.S.; Sorokoumov, V.N.; Gureev, M.A.; Kryukova, M.A.; Shpakov, A.O.; Balova, I.A. Synthesis , X-ray and DFT studies of 6-halo-3-(hydroxymethyl ) cinnolin-4(1H)-ones. Chem. Heterocycl. Compd. 2022, 58, 432–437, doi: 10.1007/s10593-022-03109-3. Impact Factor: 1.490.
- Govdi, A.I.; Tokareva, P.V.; Rumyantsev, A.M.; Panov, M.S.; Stellmacher, J.; Alexiev, U.; Danilkina, N.A.; Balova, I.A. 4,5-Bis(arylethynyl)-1,2,3-triazoles—A New Class of Fluorescent Labels: Synthesis and Applications. Molecules 2022, 27, doi: 10.3390/molecules27103191. Impact Factor: 4.927.
- Gholinejad, M.; Shojafar, M.; Sansano, J.M.; Mikhaylov, V.N.; Balova, I.A.; Khezri, R. Hyperbranched polymer immobilized palladium nanoparticles as an efficient and reusable catalyst for cyanation of aryl halides and reduction of nitroarenes. J. Organomet. Chem. 2022, 970–971, doi: 10.1016/j.jorganchem.2022.122359. Impact Factor: 2.345.
- Derkach, K. V; Fokina, E.A.; Bakhtyukov, A.A.; Sorokoumov, V.N.; Stepochkina, A.M.; Zakharova, I.O.; Shpakov, A.O. The Study of Biological Activity of a New Thieno[2,3-D]-Pyrimidine-Based Neutral Antagonist of Thyrotropin Receptor. Bull. Exp. Biol. Med. 2022, 172, 713–717, doi: 10.1007/s10517-022-05462-x. Impact Factor: 0.737.
- Bakhtyukov, A.A.; Derkach, K. V; Fokina, E.A.; Sorokoumov, V.N.; Zakharova, I.O.; Bayunova, L. V; Shpakov, A.O. Development of Low-Molecular-Weight Allosteric Agonist of Thyroid-Stimulating Hormone Receptor with Thyroidogenic Activity. Dokl. Biochem. Biophys. 2022, 503, 67–70, doi: 10.1134/S1607672922020016. Impact Factor: 0.834.
- Bakhtyukov, A.A.; Derkach, K. V; Sorokoumov, V.N.; Stepochkina, A.M.; Romanova, I. V; Morina, I.Y.; Zakharova, I.O.; Bayunova, L. V; Shpakov, A.O. The effects of separate and combined treatment of male rats with type 2 diabetes with metformin and orthosteric and allosteric agonists of luteinizing hormone receptor on steroidogenesis and spermatogenesis. Int. J. Mol. Sci. 2022, 23, doi: 10.3390/ijms23010198. Impact Factor: 6.208.
- Bakhtyukov, A.A.; Derkach, K.V.; Stepochkina, A.M.; Sorokoumov, V.N.; Bayunova, L.V.; Lebedev, I.A.; Shpakov, A.O. Effects of metformin and lutheinizing hormone receptor agonists on steroidogenesis and spermatogenesis in rats with type 2 diabetes with their separate and combined administration. Metabolism 2022, 128, 155010, doi: 10.1016/j.metabol.2021.155010. Impact Factor: 13.934.
- Bakhtyukov, A.A.; Morina, I.Y.; Derkach, K. V.; Romanova, I. V.; Sorokoumov, V.N.; Shpakov, A.O. Development of Approaches to Reducing the Effective Gonadotropin Dose in Treating Androgen Insufficiency in Male Rats with Type 1 Diabetes Mellitus. J. Evol. Biochem. Physiol. 2022, 58, 1503–1513, doi: 10.1134/S0022093022050209. Impact Factor: 1.621.
- Stepochkina, A.M.; Bakhtyukov, A.A.; Derkach, K. V.; Sorokoumov, V.N.; Shpakov, A.O. A Comparative Study of the Steroidogenic Effect of 5-Amino-N-tert-butyl-2-(methylthio)-4-(3-(nicotinamido)phenyl)thieno[2,3-d]-pyrimidine-6-carboxamide and Chorionic Gonadotropin with Different Methods of Administration to Male Rats. J. Evol. Biochem. Physiol. 2022, 58, 54–63, doi: 10.1134/S0022093022010057. Impact Factor: 1.621.
2021
- Mikhaylov, V.N.; Kazakov, I. V.; Parfeniuk, T.N.; Khoroshilova, O. V.; Scheer, M.; Timoshkin, A.Y.; Balova, I.A. The carbene transfer to strong Lewis acids: copper is better than silver. Dalt. Trans. 2021, 50, 2872–2879. doi: 10.1039/D1DT00235J.
- Efremova, M.M.; Govdi, A.I.; Frolova, V.V.; Rumyantsev, A.M.; Balova, I.A. Design and Synthesis of New 5-aryl-4-Arylethynyl-1H-1,2,3-triazoles with Valuable Photophysical and Biological Properties. Molecules. 2021, 26, 2801. doi: 10.3390/molecules26092801.
- V. N. Mikhaylov, I. A. Balova. Alternative Transformations of N-Heterocyclic Carbene Complexes of the Group 11 Metals in Transmetalation Reactions (A Review). Russian Journal of General Chemistry. 2021, Vol. 91, No. 11, pp. 2192–2246. DOI: 10.1134/S1070363221110098.
- Danilkina N.A., Govdi A.I., Khlebnikov A. F., Tikhomirov A.O. Sharoyko V. V., Shtyrov A. A., Ryazantsev M. N. Bräse S., Balova I. A. Heterocycloalkynes Fused to a Heterocyclic Core: Searching for an Island with Optimal Stability-Reactivity Balance. J. Am. Chem. Soc. 2021, 143, 16519–16537. doi: 10.1021/jacs.1c06041.
- Danilkina, N.A.; Andrievskaya, E.V.; Vasileva, A.V.; Lyapunova, A.G.; Rumyantsev, A.M.; Kuzmin, A.A.; Bessonova, E.A.; Balova, I.A. 4-Azidocinnoline—Cinnoline-4-amine Pair as a New Fluorogenic and Fluorochromic Environment-Sensitive Probe. Molecules. 2021, 26, 7460. doi: 10.3390/molecules26247460.
- A.A. Bakhtyukov, K.V. Derkach, I.V. Romanova, V.N. Sorokoumov, T.V. Sokolova, A.I. Govdi, I. Yu. Morina, A.A. Perminova, A.O. Shpakov. Effect of Low-Molecular-Weight Allosteric Agonists of the Luteinizing Hormone Receptor on Its Expression and Distribution in Rat Testes. J Evol Biochem Phys. 2021, 57, 208–220. doi: 10.1134/S0022093021020034.
- Bakhtyukov A.A., Derkach K.V., Stepochkina A.M., Sorokoumov V.N., Bayunova L.V., Lebedev I.A., Shpakov A.O. / The effect of metformin therapy on luteinizing hormone receptor agonists-induced stimulation of testosterone production and spermatogenesis in diabetic rats. J Evol Biochem Phys. 2021, V. 57. № 6. P. 1382–1393. doi: 10.1134/S002209302106017X.
- 12. Derkach, K.V., Romanova, I.V., Bakhtyukov, A.A., Morina, I.Y., Dar’in, D.V., Sorokoumov, V.N., Shpakov, A.O. / The Effect of Low-Molecular-Weight Allosteric Agonist of Luteinizing Hormone Receptor on Functional State of the Testes in Aging and Diabetic Rats. Bulletin of Experimental Biology and Medicine, 2021,171 (1), pp. 81-86. doi: 10.1007/s10517-021-05177-5.
2020
- Mikhaylov, V. N.; Pavlov, A. O.; Ogorodnov, Y. V; Spiridonova, D. V; Sorokoumov, V. N.; Balova, I. A. N-Propargylation and Copper(I)-Catalyzed Azide-Alkyne Cycloaddition as a Convenient Strategy for Directed Post-Synthetic Modification of 4-Oxo-1,4-Dihydrocinnoline Derivatives. Chem. Heterocycl. Compd. 2020, 56 (7), 915–922, doi: 10.1007/s10593-020-02750-0.
- Danilkina, N. A., D’yachenko, A., Govdi, A. I., Khlebnikov, A. F., Kornyakov, I., Bräse, S., & Balova, I. A. (2020). Intramolecular Nicholas Reactions in the Synthesis of Heteroenediynes fused to Indole, Triazole and Isocoumarin. The Journal of Organic Chemistry, doi: 10.1021/acs.joc.0c00930.
- Danilkina, N. A.; Govdi, A. I.; Balova, I. A. 5-Iodo-1H-1,2,3-triazoles as Versatile Building Blocks. Synthesis (Stuttg). 2020, 11–16, doi: 10.1055/s-0039-1690858.
- Danilkina, N. A.; Vasileva, A. A.; Balova, I. A. A.E.Favorskii’s scientific legacy in modern organic chemistry: prototropic acetyleneallene isomerization and the acetylene zipper reaction. Russ. Chem. Rev. 2020, 89, 125–171, doi: 10.1070/rcr4902.
- Mikhaylov, V. N.; Sorokoumov, V. N.; Novikov, A. S.; Melnik, M. V; Tskhovrebov, A. G.; Balova, I. A. Intramolecular hydrogen bonding stabilizes trans-configuration in a mixed carbene/isocyanide PdII complexes. J. Organomet. Chem. 2020, 121174, doi: 10.1016/j.jorganchem.2020.121174.
- Gordeychuk, D. I.; Sorokoumov, V. N.; Mikhaylov, V. N.; Panov, M. S.; Khairullina, E. M.; Melnik, M. V.; Kochemirovsky, V. A.; Balova, I. A. Copper-Based Nanocatalysts Produced via Laser-Induced Ex Situ Generation for Homo- and Cross-Coupling Reactions. Chem. Eng. Sci. 2020, 227, 115940. doi: 10.1016/j.ces.2020.115940.
2019
- Tskhovrebov, A. G.; Novikov, A. S.; Odintsova, O. V.; Mikhaylov, V. N.; Sorokoumov, V. N.; Serebryanskaya, T. V.; Starova, G. L. Supramolecular polymers derived from the PtII and PdII schiff base complexes via C(sp2)–H … Hal hydrogen bonding: Combined experimental and theoretical study. J. Organomet. Chem. 2019, 886, 71–75, doi: 10.1016/j.jorganchem.2019.01.023.
- Danilkina, N. A.; Bukhtiiarova, N. S.; Govdi, A. I.; Vasileva, A. A.; Rumyantsev, A. M.; Volkov, A. A.; Sharaev, N. I.; Povolotskiy, A. V.; Boyarskaya, I. A.; Kornyakov, I. V.; Tokareva, P. V.; Balova, I. A. Synthesis and Properties of 6-Aryl-4-azidocinnolines and 6-Aryl-4-(1,2,3-1H-triazol-1-yl)cinnolines. Molecules 2019, 24, 2386, doi: 10.3390/molecules24132386.
- Danilkina, N.; Rumyantsev, A.; Lyapunova, A.; D’yachenko, A.; Khlebnikov, A.; Balova, I. 10-Membered Azaenediyne Fused to a Benzothiophene through the Nicholas Macrocyclization: Synthesis and DNA Cleavage Ability. Synlett 2019, 30, 161–166. DOI: 10.1055/s-0037-1610352.
- Govdi, A. I.; Danilkina, N. A.; Ponomarev, A. V.; Balova, I. A. 1-Iodobuta-1,3-diynes in Copper-Catalyzed Azide–Alkyne Cycloaddition: A One-Step Route to 4-Ethynyl-5-iodo-1,2,3-triazoles. J. Org. Chem. 2019, 84, 1925–1940. DOI: 10.1021/acs.joc.8b02916.
2018
- Kulyashova, A. E.; Ponomarev, A. V.; Selivanov, S. I.; Khlebnikov, A. F.; Popik, V. V.; Balova, I. A. Cr(II)-promoted internal cyclization of acyclic enediynes fused to benzo[b]thiophene core: Macrocycles versus 2-methylenecycloalkan-1-ols formation. Arab. J. Chem. 2018. DOI: 10.1016/j.arabjc.2018.05.005.
- Mikhaylov, V.; Sorokoumov, V.; Liakhov, D.; Tskhovrebov, A.; Balova, I. Polystyrene-Supported Acyclic Diaminocarbene Palladium Complexes in Sonogashira Cross-Coupling: Stability vs. Catalytic Activity. Catalysts 2018, 8, 141. DOI: 10.3390/catal8040141.
- Tskhovrebov, A. G.; Vasileva, A. A.; Goddard, R.; Riedel, T.; Dyson, P. J.; Mikhaylov, V. N.; Serebryanskaya, T. V.; Sorokoumov, V. N.; Haukka, M. Palladium(II)-Stabilized Pyridine-2-Diazotates: Synthesis, Structural Characterization, and Cytotoxicity Studies. Inorg. Chem. 2018, 57, 930–934. DOI: 10.1021/acs.inorgchem.8b00072.
- Zakharova, I. O.; Sorokoumov, V. N.; Bayunova, L. V; Derkach, K. V; Shpakov, A. O. 4-oxo-1,4-dihydrocinnoline Derivative with Phosphatase 1B Inhibitor Activity Enhances Leptin Signal Transduction in Hypothalamic Neurons. J. Evol. Biochem. Physiol. 2018, 54, 273–280. DOI: 10.1134/S0022093018040038.
- Konovalov, A. I.; Antipin, I. S.; Burilov, V. A.; Madzhidov, T. I.; Kurbangalieva, A. R.; Nemtarev, A. V.; Solovieva, S. E.; Stoikov, I. I.; Mamedov, V. A.; Zakharova, L. Y.; Gavrilova, E. L.; Sinyashin, O. G.; Balova, I. A.; Vasilyev, A. V.; Zenkevich, I. G.; Krasavin, M. Y.; Kuznetsov, M. A.; Molchanov, A. P.; Novikov, M. S.; Nikolaev, V. A.; Rodina, L. L.; Khlebnikov, A. F.; Beletskaya, I. P.; Vatsadze, S. Z.; Gromov, S. P.; Zyk, N. V.; Lebedev, A. T.; Lemenovskii, D. A.; Petrosyan, V. S.; Nenaidenko, V. G.; Negrebetskii, V. V.; Baukov, Y. I.; Shmigol’, T. A.; Korlyukov, A. A.; Tikhomirov, A. S.; Shchekotikhin, A. E.; Traven’, V. F.; Voskresenskii, L. G.; Zubkov, F. I.; Golubchikov, O. A.; Semeikin, A. S.; Berezin, D. B.; Stuzhin, P. A.; Filimonov, V. D.; Krasnokutskaya, E. A.; Fedorov, A. Y.; Nyuchev, A. V.; Orlov, V. Y.; Begunov, R. S.; Rusakov, A. I.; Kolobov, A. V.; Kofanov, E. R.; Fedotova, O. V.; Egorova, A. Y.; Charushin, V. N.; Chupakhin, O. N.; Klimochkin, Y. N.; Osyanin, V. A.; Reznikov, A. N.; Fisyuk, A. S.; Sagitullina, G. P.; Aksenov, A. V.; Aksenov, N. A.; Grachev, M. K.; Maslennikova, V. I.; Koroteev, M. P.; Brel’, A. K.; Lisina, S. V.; Medvedeva, S. M.; Shikhaliev, K. S.; Suboch, G. A.; Tovbis, M. S.; Mironovich, L. M.; Ivanov, S. M.; Kurbatov, S. V.; Kletskii, M. E.; Burov, O. N.; Kobrakov, K. I.; Kuznetsov, D. N. Modern Trends of Organic Chemistry in Russian Universities. Russ. J. Org. Chem. 2018, 54, 157–371. DOI: 10.1134/S107042801802001X.
- Lyapunova, A. G.; Danilkina, N. A.; Rumyantsev, A. M.; Khlebnikov, A. F.; Chislov, M. V.; Starova, G. L.; Sambuk, E. V.; Govdi, A. I.; Bräse, S.; Balova, I. A. Relative Reactivity of Benzothiophene-Fused Enediynes in the Bergman Cyclization. J. Org. Chem. 2018, 83, 2788–2801. DOI: 10.1021/acs.joc.7b03258.
2017
- Shpakova, E. A.; Sorokoumov, V. N.; Akent’ev, A. V.; Derkach, K. V.; Tennikova, T. B.; Shpakov, A. O. The relationship between micelle formation and biological activity of peptide 562–572 of luteinizing hormone receptor modified with decanoyl radicals. Cell tissue biol. 2017, 11, 227–233. DOI: 10.1134/S1990519X17030105.
- Sorokoumov, V. N.; Shpakov, A. O. Protein phosphotyrosine phosphatase 1B: Structure, function, role in the development of metabolic disorders and their correction by the enzyme inhibitors. J. Evol. Biochem. Physiol. 2017, 53, 259–270. DOI: 10.1134/S0022093017040020.
- Gordeychuk, D. Vladimir Kochemirovsky, Victor Sorokoumov, Ilya Tumkin, Alexey Kuzmin, Irina Balova. Copper Particles Generated During in situ Laser-induced Synthesis Exhibit Catalytic Activity Towards Formation of Gas Phase. J. Laser Micro/Nanoengineering 2017, 12, 57–61. DOI: 10.2961/jlmn.2017.02.0001.
- Mikhaylov, V. N.; Sorokoumov, V. N.; Balova, I. A. Polystyrene-supported diaminocarbene complexes of palladium(II): synthesis, characterization and application as a precatalyst in Sonogashira–Hagihara and Suzuki–Miyaura cross coupling. Russ. Chem. Rev. 2017, 86, 459–473. DOI: 10.1070/RCR4715.
- Lyapunova, A. G.; D’yachenko, A. S.; Danilkina, N. A. Potassium fluoride for one-pot desilylation and the Sonogashira coupling of ethynylsilanes and buta-1,3-diynylsilanes. Russ. J. Org. Chem. 2017, 53, 800–804. DOI: 10.1134/S1070428017050268.
- Govdi, A. I.; Kulyashova, A. E.; Vasilevsky, S. F.; Balova, I. A. Functionalized buta-1,3-diynyl-N-methylpyrazoles by sequential “diacetylene zipper” and Sonogashira coupling reactions. Tetrahedron Lett. 2017, 58, 762–765. DOI: 10.1016/j.tetlet.2017.01.032.
2016
- Danilkina, N. A.; Gurskaya, L. Y.; Vasilyev, A. V; Balova, I. A. Towards Isocoumarin-Fused Enediyne Systems through the Electrophilic Cyclization of Methyl o-(Buta-1,3-diynyl)benzoates. European J. Org. Chem. 2016, 739–747. DOI: 10.1002/ejoc.201501262.
- Lyapunova, A. G.; Danilkina, N. A.; Khlebnikov, A. F.; Köberle, B.; Bräse, S.; Balova, I. A. Oxaenediynes through the Nicholas-Type Macrocyclization Approach. European J. Org. Chem. 2016, 2016, 4842–4851. DOI: 10.1002/ejoc.201600767.
- Mikhaylov, V. N.; Sorokoumov, V. N.; Korvinson, K. A.; Novikov, A. S.; Balova, I. A. Synthesis and Simple Immobilization of Palladium(II) Acyclic Diaminocarbene Complexes on Polystyrene Support as Efficient Catalysts for Sonogashira and Suzuki–Miyaura Cross-Coupling. Organometallics 2016, 35, 1684–1697. DOI: 10.1021/acs.organomet.6b00144.
- Mikhailov, V. N.; Korvinson, K.; Sorokoumov, V. N. Chiral acyclic diaminocarbene complexes of palladium(II) immobilized on a polymeric support as promising catalysts of the Suzuki reaction. Russ. J. Gen. Chem. 2016, 86, 2473–2476. DOI: 10.1134/S1070363216110128.
2009–2015
- Danilkina, N. A.; Vlasov, P. S.; Vodianik, S. M.; Kruchinin, A. A.; Vlasov, Y. G.; Balova, I. A. Synthesis and chemosensing properties of cinnoline-containing poly(arylene ethynylene)s. Beilstein J. Org. Chem. 2015, 11, 373–384. DOI: 10.3762/bjoc.11.43.
- Danilkina, N. A.; Lyapunova, A. G.; Khlebnikov, A. F.; Starova, G. L.; Bräse, S.; Balova, I. A. Ring-Closing Metathesis of Co2(CO)6–Alkyne Complexes for the Synthesis of 11-Membered Dienediynes: Overcoming Thermodynamic Barriers. J. Org. Chem. 2015, 80, 5546–5555. DOI: 10.1021/acs.joc.5b00409.
- Kulyashova, A. E.; Mikheeva, E. V.; Danilkina, N. A.; Balova, I. A. Synthesis of 2-(buta-1,3-diynyl)-N,N-dimethylanilines Using Reductive Methylation Step. Mendeleev Commun. 2014, 24, 102–104. DOI: 10.1016/j.mencom.2014.03.013.
- Danilkina, N. A.; Kulyashova, A. E.; Khlebnikov, A. F.; Bräse, S.; Balova, I. A. Electrophilic Cyclization of Aryldiacetylenes in the Synthesis of Functionalized Enediynes Fused to a Heterocyclic Core. J. Org. Chem. 2014, 79, 9018–9045. DOI: 10.1021/jo501396s.
- Mikhailov, V. N.; Savicheva, E. A.; Sorokoumov, V. N.; Boyarskii, V. P. Catalytic activity of palladium(II) diaminocarbene complexes in the Sonogashira and Suzuki reactions. Russ. J. Org. Chem. 2013, 49, 551–554. DOI: 10.1134/S107042801304009X.
- Ryabukhin, D. S.; Sorokoumov, V. N.; Savicheva, E. A.; Boyarskiy, V. P.; Balova, I. A.; Vasilyev, A. V. Catalytic activity of palladium acyclic diaminocarbene complexes in the synthesis of 1,3-diarylpropynones via Sonogashira reaction: cross- versus homo-coupling. Tetrahedron Lett. 2013, 54, 2369–2372. DOI: 10.1016/j.tetlet.2013.02.086.
- Kulyashova, A. E.; Sorokoumov, V. N.; Popik, V. V; Balova, I. A. An acetylene zipper—Sonogashira reaction sequence for the efficient synthesis of conjugated arylalkadiynols. Tetrahedron Lett. 2013, 54, 2235–2238. DOI: 10.1016/j.tetlet.2013.02.066.
- Danilkina, N. A.; Kulyashova, A. E.; Balova, I. A. Intramolecular cyclizations of functionalized diynes. Chem. Heterocycl. Compd. 2012, 48, 95–106. DOI: 10.1007/s10593-012-0973-7.
- Danilkina, N.; Nieger, M.; Selivanov, S.; Bräse, S.; Balova, I. Electrophilic Cyclization and Ring-Closing Metathesis as Key Steps in the Synthesis of a 12-Membered Cyclic Enediyne. European J. Org. Chem. 2012, 2012, 5660–5664. DOI: 10.1002/ejoc.201200881.
- Danilkina, N. A.; Gorbunova, E. G.; Sorokoumov, V. N.; Balova, I. A. Study of cyclyzation of o-(1-Alkynyl)- and o-(1,3-Butadiynyl)aryltriazenes under the action of acids. Russ. J. Org. Chem. 2012, 48, 1424–1434. DOI: 10.1134/S1070428012110048.
- Danilkina, N. A.; Mikhaylov, L. E.; Ivin, B. A. Reaction of acetylenedicarboxylic acids esters with 4,5-dihydro-1H-pyrazole-1-carbothioamides and 3,4,5,6-tetrahydro-2H-1,2,4-triazepine-3-thiones. Chem. Heterocycl. Compd. 2011, 47, 886–900. DOI: 10.1007/s10593-011-0850-9.
- Novikov, R. V.; Danilkina, N. A.; Balova, I. A. Cyclocondensation of n-(prop-2-yn-1-yl)- and n-(penta-2,4-diyn-1-yl)- o-phenylenediamines with phenyl isothiocyanate and carbon disulfide. Chem. Heterocycl. Compd. 2011, 47, 758–766. DOI: 10.1007/s10593-011-0831-z.
- Sorokoumov, V. N.; Popik, V. V.; Balova, I. A. Access to 2,3-bis(buta-1,3-diynyl)pyridines. Mendeleev Commun. 2011, 21, 19–20. DOI: 10.1016/j.mencom.2011.01.008.
- Tskhovrebov, A. G.; Luzyanin, K. V.; Kuznetsov, M. L.; Sorokoumov, V. N.; Balova, I. A.; Haukka, M.; Kukushkin, V. Y. Substituent R-Dependent Regioselectivity Switch in Nucleophilic Addition of N-Phenylbenzamidine to PdII- and PtII-Complexed Isonitrile RN≡C Giving Aminocarbene-Like Species. Organometallics 2011, 30, 863–874. DOI: 10.1021/om101041g.
- Danilkina, N.; Bräse, S.; Balova, I. Electrophilic Cyclization of Buta-1,3-diynylarenes: Synthesis of Precursors of (Z)-3-Ene-1,5-diyne Systems Fused to Heterocycles. Synlett 2011, 2011, 517–520. DOI: 10.1055/s-0030-1259547.
- Vinogradova, O. V.; Sorokoumov, V. N.; Balova, I. A. A short route to 3-alkynyl-4-bromo(chloro)cinnolines by Richter-type cyclization of ortho-(dodeca-1,3-diynyl)aryltriaz-1-enes. Tetrahedron Lett. 2009, 50, 6358–6360. DOI: 10.1016/j.tetlet.2009.08.103.




